آیا پارکینسون بیماری خود ایمنی است ؟ ۳ کشف مهم که باید بدانید
بیماری پارکینسون برای دههها به عنوان یک بیماری تخریب عصبی شناخته میشد؛ اختلالی که در آن سلولهای حیاتی مغز به تدریج از بین میروند و منجر به علائم حرکتی ناتوانکنندهای مانند لرزش، کندی حرکت و سفتی عضلات میشود. تمرکز اصلی علم پزشکی بر درک چگونگی تجمع پروتئینهای سمی در مغز و مرگ سلولهای تولیدکننده دوپامین بود. اما در سالهای اخیر، یک تغییر پارادایم واقعی در حال وقوع است؛ دیدگاهی جدید و هیجانانگیز که نقش یک بازیگر قدرتمند دیگر را در این سناریو پررنگ میکند: سیستم ایمنی بدن.
این نگاه نو، پارکینسون را از یک بیماری که تصور میشد صرفاً محدود به سیستم عصبی است، به یک اختلال پیچیده با ابعاد چندگانه تبدیل کرده است. شواهد علمی فزایندهای نشان میدهند که سیستم ایمنی، که وظیفهاش دفاع از بدن در برابر مهاجمان خارجی است، ممکن است در بیماری پارکینسون به اشتباه علیه سلولهای خودی مغز وارد عمل شود. این فرضیه سوالی بنیادین را مطرح میکند: آیا پارکینسون صرفاً یک بیماری تخریب عصبی است یا میتوان آن را یک بیماری با مولفههای خودایمنی قوی در نظر گرفت؟ پاسخ به این سوال نه تنها درک ما از این بیماری را متحول میکند، بلکه میتواند مسیرهای درمانی کاملاً جدیدی را برای میلیونها بیمار در سراسر جهان باز کند و به آنها و خانوادههایشان امید تازهای ببخشد.
سلب مسئولیت مهم توجه: اطلاعات ارائه شده در این مقاله صرفاً جنبه آموزشی دارد و نباید جایگزین مشاوره، تشخیص یا درمان حرفهای پزشکی شود. برای ارزیابی دقیق شرایط خود و دریافت راهنماییهای درمانی، همواره با پزشک یا متخصص مغز و اعصاب مشورت کنید.
نکات کلیدی در یک نگاه
- درک کلاسیک: پارکینسون به طور سنتی یک بیماری تخریب عصبی است که علت اصلی آن تجمع سمی پروتئین “آلفا-سینوکلئین” و مرگ سلولهای مغزی تولیدکننده دوپامین است.
- شواهد جدید: تحقیقات علمی قوی، از جمله وجود التهاب عصبی مزمن، حمله مستقیم سلولهای ایمنی (لنفوسیتهای T) به نورونها و ارتباطات ژنتیکی مشترک، به نقش کلیدی سیستم ایمنی در پیشرفت بیماری اشاره دارند.
- طبقهبندی فعلی: در حال حاضر، پارکینسون رسماً به عنوان یک بیماری خودایمنی طبقهبندی نمیشود. با این حال، جامعه علمی آن را به عنوان یک بیماری “با مولفههای خودایمنی قوی” به رسمیت میشناسد که در آن پاسخ ایمنی، نقش مهمی در تشدید و پیشرفت آسیب عصبی ایفا میکند.
- چشمانداز آینده: این دیدگاه جدید، افقهای درمانی نویدبخشی مانند ایمونوتراپی را برای کنترل یا کند کردن روند بیماری باز کرده است.
پارکینسون چیست؟ مروری بر یک بیماری پیچیده عصبی
برای درک ارتباط پارکینسون با سیستم ایمنی، ابتدا باید با ماهیت اصلی این بیماری و پیچیدگیهای آن عمیقتر آشنا شویم.
تعریف کلاسیک: تجمع آلفا-سینوکلئین و مرگ سلولهای دوپامینرژیک
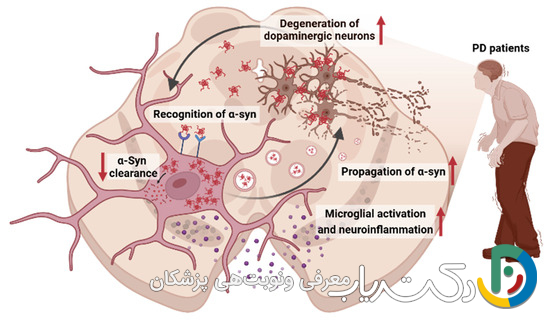
در قلب پاتولوژی بیماری پارکینسون، مرگ پیشرونده سلولهای عصبی (نورونها) در ناحیهای از مغز میانی به نام توده سیاه قرار دارد. این سلولها مسئول تولید یک ماده شیمیایی حیاتی به نام دوپامین هستند. دوپامین یک انتقالدهنده عصبی است که نقشی کلیدی در کنترل حرکات روان و هماهنگ بدن از طریق مداری به نام عقدههای قاعدهای ایفا میکند. این مدارها برای شروع حرکات ارادی، تنظیم سرعت و دامنه آنها و جلوگیری از حرکات ناخواسته ضروری هستند.
علت اصلی مرگ این سلولها، تجمع غیرطبیعی و تودهای یک پروتئین به نام آلفا-سینوکلئین است. در حالت عادی، این پروتئین در انتهای نورونها وجود دارد و در آزادسازی انتقالدهندههای عصبی نقش دارد. اما در پارکینسون، این پروتئین دچار تاخوردگی اشتباه شده و به هم میچسبد و ساختارهای سمی و نامحلولی به نام اجسام لویی را تشکیل میدهد. این تودههای پروتئینی عملکرد طبیعی سلولهای عصبی را مختل کرده، به غشای سلولی و اندامکهای حیاتی مانند میتوکندری (نیروگاه سلول) آسیب میزنند و در نهایت منجر به مرگ آنها میشوند. با کاهش سطح دوپامین، مدارهای مغزی مسئول کنترل حرکت دچار اختلال شده و علائم حرکتی پارکینسون ظاهر میشوند. طبق آمار، پارکینسون پس از آلزایمر، دومین بیماری شایع تخریب عصبی در جهان است و بیش از ۱۰ میلیون نفر را تحت تأثیر قرار داده است.
علائم حرکتی و غیرحرکتی: فراتر از لرزش
اگرچه پارکینسون بیشتر با علائم حرکتی شناخته میشود، اما یک بیماری بسیار گستردهتر است که تمام جنبههای زندگی فرد را تحت تأثیر قرار میدهد.
- علائم حرکتی اصلی:
- لرزش در حالت استراحت : این لرزش ریتمیک که اغلب به صورت “قرص غلتاندن” بین انگشت شست و اشاره توصیف میشود، معمولاً از یک دست شروع شده و در زمان استراحت بیشتر مشهود است و با انجام یک حرکت ارادی کاهش مییابد.
- کندی حرکت : این علامت یکی از ناتوانکنندهترین جنبههای بیماری است. فرد در شروع حرکت دچار مشکل میشود و حرکاتش آهسته، کوچک و ناقص به نظر میرسد. این وضعیت در فعالیتهای روزمره مانند راه رفتن (که منجر به گامهای کوتاه میشود)، نوشتن (که باعث ریز شدن دستخط یا میکروگرافیا میشود) و حتی تغییر حالت چهره (که به آن صورت ماسک میگویند) خود را نشان میدهد.
- سفتی عضلات : مقاومت عضلات در برابر حرکت که میتواند باعث درد، گرفتگی و محدودیت دامنه حرکتی شود. این سفتی اغلب در گردن، شانهها و اندامها احساس میشود.
- بیثباتی در وضعیت بدن : این علامت که معمولاً در مراحل پیشرفتهتر بیماری ظاهر میشود، به مشکلات تعادل و هماهنگی اشاره دارد و خطر زمین خوردن را به شدت افزایش میدهد.
- علائم غیرحرکتی: این علائم که اغلب سالها و حتی دههها قبل از بروز مشکلات حرکتی شروع میشوند، ناشی از گسترش پاتولوژی اجسام لویی به سایر نواحی مغز و سیستم عصبی محیطی هستند.
- از دست دادن حس بویایی : یکی از اولین و شایعترین علائم غیرحرکتی است که به دلیل تجمع اجسام لویی در پیاز بویایی مغز رخ میدهد.
- اختلالات خواب: شامل بیخوابی، خوابآلودگی شدید در طول روز و به خصوص اختلال رفتار خواب REM که در آن فرد رویاهای خود را به صورت فیزیکی اجرا میکند (فریاد زدن، لگد زدن در خواب) و میتواند نشانه اولیه قوی برای پارکینسون باشد.
- مشکلات گوارشی: یبوست مزمن بسیار شایع است و به دلیل درگیری سیستم عصبی روده (سیستم عصبی انتریک) رخ میدهد.
- مشکلات خلقی و شناختی: افسردگی و اضطراب در بیش از نیمی از بیماران دیده میشود. در مراحل پیشرفتهتر، مشکلات شناختی مانند کندی تفکر، مشکلات حافظه و در نهایت دمانس (زوال عقل) ممکن است بروز کند.
سیستم ایمنی و خودایمنی: یک شمشیر دولبه
سیستم ایمنی بدن یک شبکه پیچیده و هوشمند از سلولها و مولکولهاست که برای محافظت از ما در برابر عوامل بیماریزا مانند ویروسها، باکتریها و انگلها طراحی شده است. این سیستم به دو شاخه اصلی تقسیم میشود: سیستم ایمنی ذاتی که اولین خط دفاعی سریع و غیراختصاصی است و سیستم ایمنی تطبیقی که دفاعی آهستهتر اما بسیار دقیق و هدفمند را فراهم میکند و حافظه ایمنی ایجاد میکند.
بیماری خودایمنی چیست؟ وقتی بدن به خود حمله میکند
در شرایط عادی، سیستم ایمنی به بافتها و سلولهای بدن حمله نمیکند. اما در بیماریهای خودایمنی ، این سیستم دچار خطا شده و به اشتباه سلولها، بافتها یا اندامهای سالم خودی را به عنوان یک تهدید شناسایی کرده و به آنها حمله میکند. این حمله منجر به التهاب مزمن و آسیب بافتی میشود. در این فرآیند، سلولهای T به طور مستقیم به سلولهای خودی حمله میکنند و سلولهای B، آنتیبادیهایی به نام اتوآنتیبادی تولید میکنند که به ساختارهای خودی متصل شده و آنها را برای تخریب علامتگذاری میکنند. بیماریهایی مانند اماس ، آرتریت روماتوئید و دیابت نوع ۱ نمونههای شناختهشدهای از اختلالات خودایمنی هستند.
شواهد ارتباط بین پارکینسون و سیستم ایمنی
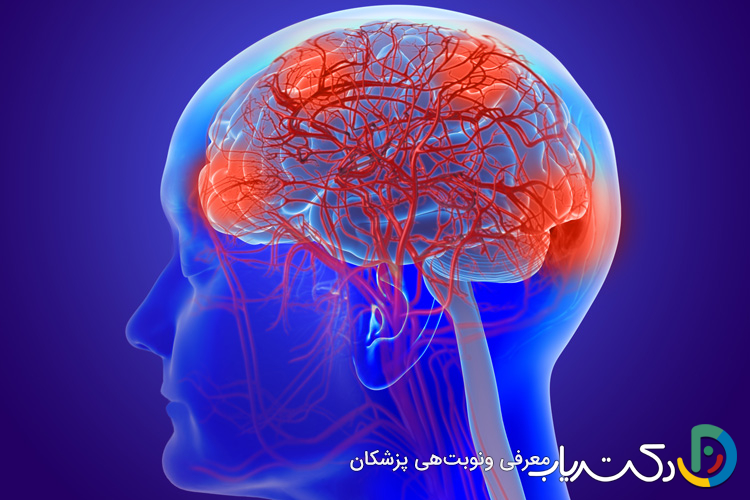
اکنون این سوال مطرح میشود که چه شواهدی باعث شده دانشمندان به نقش سیستم ایمنی در پارکینسون مشکوک شوند؟ این شواهد از سه حوزه اصلی به دست آمدهاند:
۱. التهاب عصبی : یک ویژگی کلیدی در مغز بیماران پارکینسون
کالبدشکافی مغز بیماران مبتلا به پارکینسون نشان داده است که در نواحی آسیبدیده، سلولهای ایمنی مقیم مغز که میکروگلیا و آستروسیتها نام دارند، به طور مزمن فعال هستند. این سلولهای فعال، مولکولهای التهابی قدرتمندی به نام سیتوکین مانند TNF-alpha و اینترلوکین-۱ بتا آزاد میکنند.
در حالی که التهاب حاد یک پاسخ دفاعی طبیعی است، التهاب مزمن در مغز یک چرخه معیوب و ویرانگر ایجاد میکند:
- تجمع آلفا-سینوکلئین باعث فعال شدن میکروگلیا میشود.
- میکروگلیا با تولید سیتوکینهای التهابی باعث ایجاد استرس اکسیداتیو و آسیب مستقیم به نورونها میشوند.
- این التهاب همچنین میتواند به سد خونی-مغزی آسیب برساند، سدی که به طور معمول از ورود سلولهای ایمنی از جریان خون به مغز جلوگیری میکند.
- با نفوذپذیر شدن این سد، سلولهای ایمنی محیطی (مانند لنفوسیتهای T) وارد مغز شده و به آتش التهاب دامن میزنند.
- مرگ نورونها منجر به آزاد شدن بیشتر آلفا-سینوکلئین و تشدید پاسخ التهابی میگردد. این التهاب عصبی هم علت و هم معلول تخریب عصبی در پارکینسون است.
۲. نقش سلولهای T در حمله به نورونها
یکی از پیشگامانهترین اکتشافات در این زمینه، مطالعهای بود که در سال ۲۰۱۷ در مجله معتبر Nature منتشر شد. محققان دریافتند که لنفوسیتهای T (نوعی سلول کلیدی در سیستم ایمنی تطبیقی) در خون بیماران پارکینسون، قطعاتی از پروتئین آلفا-سینوکلئین را به عنوان یک عامل بیگانه شناسایی میکنند. این شناسایی از طریق گیرندههایی روی سطح سلولهای T انجام میشود که به قطعات پروتئینی ارائهشده توسط مولکولهای MHC (Major Histocompatibility Complex) متصل میشوند.
این یافته به این معناست که سیستم ایمنی این بیماران، پروتئین خودی مغز را با یک مهاجم خارجی اشتباه گرفته و سلولهای T را برای حمله به نورونهایی که این پروتئین را تولید میکنند (یعنی نورونهای دوپامینرژیک) بسیج میکند. این کشف، یکی از قویترین شواهد مستقیم برای وجود یک پاسخ خودایمنی در بیماری پارکینسون است، زیرا نشان میدهد که سیستم ایمنی تطبیقی به طور فعال در هدف قرار دادن و تخریب سلولهای عصبی نقش دارد.
۳. ارتباط ژنتیکی: ژنهای مشترک بین پارکینسون و بیماریهای خودایمنی
تحقیقات ژنتیکی نیز ارتباط قانعکنندهای را نشان دادهاند. مشخص شده است که برخی از ژنهایی که خطر ابتلا به پارکینسون را افزایش میدهند، در تنظیم سیستم ایمنی نیز نقش دارند.
- ژن LRRK2: جهش در این ژن یکی از شایعترین علل ژنتیکی پارکینسون است. همین ژن با بیماریهای التهابی و خودایمنی مانند بیماری کرون نیز ارتباط دارد.
- ژنهای HLA: مطالعات گسترده ژنومی نشان دادهاند که واریانتهای خاصی در ناحیه ژنی HLA (Human Leukocyte Antigen)، که برای عملکرد سیستم ایمنی تطبیقی حیاتی هستند و قویترین ارتباط ژنتیکی را با بیماریهای خودایمنی کلاسیک دارند، با افزایش خطر ابتلا به پارکینسون نیز مرتبط هستند.
این همپوشانی ژنتیکی نشان میدهد که یک استعداد ذاتی برای اختلال در عملکرد سیستم ایمنی ممکن است فرد را هم در معرض خطر پارکینسون و هم سایر بیماریهای خودایمنی قرار دهد.
| ویژگی ایمونولوژیک | بیماری پارکینسون | بیماری اماس (یک بیماری خودایمنی کلاسیک) |
|---|---|---|
| سلول/بافت هدف | نورونهای تولیدکننده دوپامین در توده سیاه | غلاف میلین (پوشش محافظتی رشتههای عصبی) |
| آنتیژن هدف | پروتئین آلفا-سینوکلئین | پروتئینهای موجود در غلاف میلین |
| سلولهای ایمنی اصلی | لنفوسیتهای T، میکروگلیا | لنفوسیتهای T و B |
| مکانیسم اصلی آسیب | التهاب عصبی، سمیت سلولی مستقیم | تخریب میلین (Demyelination)، آسیب آکسونی |
| نقش ژنتیک | ژنهای مشترک با بیماریهای التهابی (مانند LRRK2, HLA) | ارتباط قوی با ژنهای سیستم ایمنی (HLA) |
آیا پارکینسون رسماً یک بیماری خودایمنی طبقهبندی میشود؟
با وجود تمام این شواهد، پاسخ کوتاه به این سوال در حال حاضر “خیر” است.
دیدگاه فعلی جامعه علمی: یک بیماری “با مولفههای خودایمنی”
اگرچه نقش سیستم ایمنی غیرقابل انکار است، اما هنوز اجماع علمی برای طبقهبندی پارکینسون به عنوان یک بیماری خودایمنی اولیه وجود ندارد. بحث اصلی، یک معمای “مرغ یا تخممرغ” است: آیا پاسخ ایمنی عامل شروعکننده بیماری است یا یک عامل ثانویه و تشدیدکننده قدرتمند؟
در اکثر بیماریهای خودایمنی کلاسیک، حمله سیستم ایمنی رویداد اصلی و آغازگر بیماری است و اغلب با وجود اتوآنتیبادیهای مشخص در خون همراه است. اما در پارکینسون، به نظر میرسد که پاتولوژی اولیه، تجمع غیرطبیعی پروتئین آلفا-سینوکلئین است و پاسخ خودایمنی متعاقباً و در واکنش به این تجمع پروتئینی فعال میشود و روند تخریب عصبی را تسریع میکند. بنابراین، جامعه علمی ترجیح میدهد از پارکینسون به عنوان یک بیماری تخریب عصبی با مولفهها یا ویژگیهای خودایمنی قوی یاد کند.
پیامدهای درمانی این فرضیه: نگاهی به آینده
مهم: قبل از هرگونه اقدام درمانی، حتماً با پزشک یا داروساز خود مشورت کنید.
درک نقش سیستم ایمنی در پارکینسون، صرفاً یک کنجکاوی علمی نیست، بلکه پیامدهای درمانی بسیار مهمی دارد و راههای جدیدی را برای مقابله با این بیماری پیش روی ما قرار داده است.
داروهای تعدیلکننده سیستم ایمنی
به جای داروهای سرکوبکننده کلی سیستم ایمنی که میتوانند فرد را در برابر عفونتها آسیبپذیر کنند، محققان در حال بررسی داروهایی هستند که پاسخ ایمنی را به شکلی هوشمندانهتر تنظیم یا تعدیل میکنند. برای مثال، داروهای مهارکننده سیتوکینهای خاص مانند TNF-alpha که در درمان آرتریت روماتوئید استفاده میشوند، در مدلهای حیوانی پارکینسون نتایج امیدوارکنندهای نشان دادهاند. چندین کارآزمایی بالینی در حال انجام است تا ایمنی و اثربخشی این داروها را در کاهش التهاب عصبی و کند کردن پیشرفت بیماری پارکینسون ارزیابی کنند.
ایمونوتراپی هدفمند: رویکردی دقیقتر
این رویکرد حتی از این هم فراتر میرود. هدف ایمونوتراپی هدفمند، طراحی درمانهایی است که به طور خاص اجزای مشکلساز سیستم ایمنی را هدف قرار میدهند، بدون اینکه به عملکرد دفاعی کلی آن آسیب برسانند. دو استراتژی اصلی در این زمینه عبارتند از:
- واکسنهای درمانی: طراحی واکسنهایی که به سیستم ایمنی آموزش میدهند تا تودههای سمی پروتئین آلفا-سینوکلئین را شناسایی کرده و آنها را پاکسازی کند. این رویکرد به دو صورت ایمنسازی فعال (تزریق آنتیژن برای تحریک پاسخ ایمنی خود بیمار) و ایمنسازی غیرفعال (تزریق آنتیبادیهای از پیش ساخته شده) در حال بررسی است.
- درمانهای سلولی: توسعه روشهایی برای مهار یا حذف اختصاصی لنفوسیتهای T که به نورونهای دوپامینرژیک حمله میکنند. این میتواند شامل تکنیکهای پیشرفتهای مانند مهندسی سلولهای T تنظیمکننده برای سرکوب پاسخ خودایمنی باشد.
این رویکردها که در مرز دانش قرار دارند، امید زیادی را برای دستیابی به درمانهایی ایجاد کردهاند که نه تنها علائم، بلکه علت اصلی پیشرفت بیماری را هدف قرار میدهند.
پرسشهای متداول
۱. آیا رژیم غذایی ضدالتهابی به بیماران پارکینسون کمک میکند؟ بله، شواهد نشان میدهد که رژیمهای سرشار از آنتیاکسیدانها و ترکیبات ضدالتهابی میتوانند مفید باشند. رژیم مدیترانهای که غنی از میوهها، سبزیجات، غلات کامل، ماهی و چربیهای سالم (مانند روغن زیتون) است و مصرف گوشت قرمز و غذاهای فرآوریشده در آن کم است، میتواند به کاهش التهاب عمومی بدن و حمایت از سلامت مغز کمک کند.
۲. چه تفاوتی بین نقش سیستم ایمنی در پارکینسون و آلزایمر وجود دارد؟ هر دو بیماری با التهاب عصبی مزمن و فعالیت میکروگلیا همراه هستند. اما پروتئینهای هدف متفاوتند (آلفا-سینوکلئین در پارکینسون و آمیلوئید بتا و تاو در آلزایمر). به نظر میرسد در پارکینسون، نقش سیستم ایمنی تطبیقی (سلولهای T) برجستهتر و مستقیمتر باشد، در حالی که در آلزایمر، تمرکز بیشتری بر روی سیستم ایمنی ذاتی (میکروگلیا) وجود دارد.
۳. آیا عفونتها میتوانند خطر ابتلا به پارکینسون را افزایش دهند؟ این یک فرضیه فعال در تحقیقات است که به آن تقلید مولکولی میگویند. بر اساس این نظریه، شباهت ساختاری بین پروتئینهای یک عامل عفونی (مانند ویروس) و یک پروتئین خودی (مانند آلفا-سینوکلئین) میتواند باعث شود که پاسخ ایمنی علیه عامل عفونی، به اشتباه به پروتئین خودی نیز حمله کند و یک واکنش خودایمنی را در افراد مستعد ژنتیکی کلید بزند.
۴. آیا استرس میتواند علائم پارکینسون را تشدید کند؟ بله، استرس روانی و فیزیکی میتواند با آزاد کردن هورمونهایی مانند کورتیزول، بر عملکرد سیستم ایمنی تأثیر گذاشته و التهاب را افزایش دهد. این امر میتواند به طور موقت عملکرد مدارهای حرکتی مغز را مختل کرده و علائم حرکتی و غیرحرکتی را بدتر کند. بسیاری از بیماران گزارش میدهند که علائم آنها در دورههای استرس شدید، به وضوح تشدید میشود.
۵. آیا داروهای فعلی پارکینسون (مانند لوودوپا) بر سیستم ایمنی تأثیر میگذارند؟ داروهای استاندارد فعلی مانند لوودوپا عمدتاً برای جایگزینی دوپامین از دست رفته و مدیریت علائم حرکتی طراحی شدهاند و تأثیر مستقیم قابل توجهی بر تعدیل سیستم ایمنی ندارند. به همین دلیل است که تحقیقات جدید بر روی داروهایی با مکانیسمهای ایمنی متمرکز شدهاند تا بتوانند روند پیشرفت بیماری را هدف قرار دهند.
راهکارهای نهایی برای درک بهتر بیماری پارکینسون
درک ما از بیماری پارکینسون در حال یک تکامل عمیق است. این بیماری دیگر صرفاً یک اختلال حرکتی ناشی از کمبود دوپامین نیست، بلکه یک بیماری چندوجهی و سیستمیک است که در آن تعامل پیچیدهای بین ژنتیک، عوامل محیطی، تجمع پروتئین، استرس اکسیداتیو، التهاب عصبی و پاسخهای خودایمنی، سرنوشت سلولهای مغز را رقم میزند. اگرچه پارکینسون هنوز به طور رسمی یک بیماری خودایمنی نامیده نمیشود، اما پذیرش نقش حیاتی سیستم ایمنی در پیشرفت آن، انقلابی در رویکردهای درمانی آینده ایجاد کرده است.
اگر شما یا یکی از عزیزانتان با علائم پارکینسون مواجه هستید، برداشتن اولین قدم یعنی مشورت با یک متخصص مغز و اعصاب، حیاتی است. تشخیص دقیق و درک جامع از شرایط شما، کلید مدیریت موثر بیماری و بهبود کیفیت زندگی است. این دانش جدید به بیماران قدرت میدهد تا فعالانه در مدیریت بیماری خود شرکت کرده و با امید به آیندهای روشنتر، مسیر درمانی خود را طی کنند.
منابع
- National Institute of Neurological Disorders and Stroke (NINDS). (2023). Parkinson’s Disease Information Page. https://www.ninds.nih.gov/health-information/disorders/parkinsons-disease
- Mayo Clinic. (2022). Parkinson’s Disease. https://www.mayoclinic.org/diseases-conditions/parkinsons-disease/symptoms-causes/syc-20376055
- Parkinson’s Foundation. The Immune System and Parkinson’s Disease.
https://www.parkinson.org/blog/research/meet-dr-wallings
لیست پزشکان مرتبط:
- طیبه عباسیونمتخصص مغز و اعصاب (نورولوژی) | تهران
- مهدی سخابخشمتخصص مغز و اعصاب (نورولوژی) | تهران
- بابک زمانیمتخصص مغز و اعصاب (نورولوژی) | تهران
- رویا ابوالفضلیمتخصص مغز و اعصاب (نورولوژی) | تهران
- علیرضا رنجبر نائینیمتخصص مغز و اعصاب (نورولوژی) | تهران
- سید سهراب هاشمی فشارکیمتخصص مغز و اعصاب (نورولوژی) | تهران
- کلینیک مغز و اعصاب نورالیکلینیک مغز و اعصاب و نوروساینس | تهران
- ساناز معصومیمتخصص مغز و اعصاب (نورولوژی) | تهران
- مهران مهیارمتخصص مغز و اعصاب (نورولوژی) | تهران
- فاطمه شعبانیمتخصص مغز و اعصاب (نورولوژی) | تهران