آیا بیماری پارکینسون درمان قطعی دارد ؟ خیر (بهترین روش های مدیریت)

آیا بیماری پارکینسون قابل درمان است؟ نگاهی جامع به روشهای درمانی و مدیریت بیماری
بیماری پارکینسون، یک اختلال عصبی پیشرونده که میلیونها نفر را در سراسر جهان تحت تأثیر قرار داده است، اغلب با یک سؤال اساسی و حیاتی همراه است: آیا این بیماری قابل درمان است؟ این پرسش، که در ذهن بیماران، خانوادههایشان و عموم مردم طنینانداز میشود، نیازمند پاسخی دقیق، شفاف و مبتنی بر شواهد علمی است. در حالی که لرزش دستها شاید شناختهشدهترین علامت پارکینسون باشد، تأثیرات این بیماری بسیار فراتر رفته و جنبههای مختلفی از حرکت، تعادل، خلقوخو و کیفیت کلی زندگی را در بر میگیرد. این بیماری که برای اولین بار در سال ۱۸۱۷ توسط دکتر جیمز پارکینسون توصیف شد، امروزه به عنوان دومین بیماری شایع نورودژنراتیو پس از آلزایمر شناخته میشود و چالشهای عمیقی را برای سیستمهای بهداشتی و خانوادهها ایجاد میکند.
درک ماهیت پارکینسون و چشمانداز درمانی آن اولین گام برای مدیریت مؤثر این بیماری پیچیده است. پیشرفتهای چشمگیر علم پزشکی در دهههای اخیر، افقهای جدیدی را برای کنترل علائم و بهبود زندگی بیماران گشوده است. دیگر دوران نگاه ناامیدانه به پارکینسون به سر آمده و امروزه با رویکردهای چندجانبه، میتوان این بیماری را به گونهای مدیریت کرد که فرد بتواند سالهای متمادی به زندگی فعال و پربار خود ادامه دهد. این مقاله با هدف ارائه یک راهنمای جامع و معتبر، به بررسی عمیق روشهای درمانی موجود، استراتژیهای مدیریتی و آخرین تحقیقات علمی در زمینه بیماری پارکینسون میپردازد تا به این سؤال مهم، پاسخی روشن و همهجانبه ارائه دهد.
سلب مسئولیت مهم پزشکی (Disclaimer) اطلاعات ارائه شده در این مقاله صرفاً برای اهداف آموزشی و اطلاعرسانی است و هرگز نباید به عنوان جایگزینی برای مشاوره، تشخیص یا درمان حرفهای پزشکی در نظر گرفته شود. تشخیص و درمان بیماری پارکینسون نیازمند ارزیابی دقیق توسط پزشک متخصص مغز و اعصاب است. لطفاً برای دریافت راهنماییهای متناسب با شرایط فردی خود، همواره با پزشک یا سایر متخصصان واجد شرایط بهداشتی مشورت کنید.
نکات کلیدی در یک نگاه
- عدم وجود درمان قطعی: در حال حاضر، هیچ درمان قطعی برای ریشهکن کردن بیماری پارکینسون وجود ندارد. تحقیقات برای یافتن چنین درمانی به شدت ادامه دارد.
- تمرکز بر مدیریت علائم: هدف اصلی درمانهای فعلی، کنترل و مدیریت علائم حرکتی و غیرحرکتی بیماری به منظور حفظ استقلال و بهبود کیفیت زندگی بیماران است.
- رویکرد درمانی جامع: مؤثرترین استراتژی مدیریتی، ترکیبی از درمانهای دارویی، توانبخشی (فیزیوتراپی، کاردرمانی، گفتاردرمانی)، تغییرات سبک زندگی (تغذیه و ورزش) و در موارد پیشرفته، گزینههای جراحی مانند تحریک عمیق مغز (DBS) است.
- اهمیت تشخیص زودهنگام: شروع به موقع درمان میتواند به کنترل بهتر علائم در طولانیمدت کمک شایانی کند و از بروز برخی عوارض جلوگیری نماید.
- امید به آینده: پیشرفتهای علمی در زمینههای ژندرمانی، سلولهای بنیادی و ایمونوتراپی، امیدهای جدیدی را برای یافتن درمانهایی که بتوانند روند پیشرفت بیماری را کند یا متوقف کنند، ایجاد کرده است.
بیماری پارکینسون چیست؟ نگاهی عمیقتر به مغز
بیماری پارکینسون یک اختلال نورودژنراتیو (neurodegenerative) است؛ به این معنی که با تخریب و مرگ تدریجی سلولهای عصبی (نورونها) در یک ناحیه خاص از مغز به نام جسم سیاه (Substantia Nigra) مشخص میشود. این ناحیه بخشی از ساختار بزرگتری به نام عقدههای قاعدهای (Basal Ganglia) است که به عنوان مرکز کنترل حرکات پیچیده و هماهنگ بدن عمل میکند. سلولهای جسم سیاه مسئول تولید یک ماده شیمیایی حیاتی به نام دوپامین هستند.
دوپامین یک انتقالدهنده عصبی است که نقش یک پیامرسان کلیدی را بین جسم سیاه و سایر بخشهای مغز برای کنترل و هماهنگی حرکات بدن ایفا میکند. میتوان عملکرد دوپامین را به روغن در یک موتور تشبیه کرد؛ همانطور که روغن باعث حرکت نرم و روان قطعات موتور میشود، دوپامین نیز به مغز اجازه میدهد تا دستورات حرکتی را به صورت روان، دقیق و کنترلشده به عضلات ارسال کند. با پیشرفت پارکینسون و از بین رفتن سلولهای تولیدکننده دوپامین، سطح این ماده شیمیایی در مغز کاهش مییابد. این کمبود دوپامین است که منجر به بروز علائم حرکتی اصلی بیماری، مانند لرزش، کندی حرکات و سفتی عضلات میشود. یکی از مشخصههای پاتولوژیک کلیدی در مغز بیماران پارکینسون، وجود تودههای پروتئینی غیرطبیعی به نام اجسام لویی (Lewy Bodies) در داخل نورونهای باقیمانده است که عمدتاً از پروتئین تاخوردهای به نام آلفا-سینوکلئین تشکیل شدهاند و به نظر میرسد در فرآیند مرگ سلولی نقش دارند.
علائم اصلی و ثانویه پارکینسون: فراتر از لرزش
علائم پارکینسون معمولاً به تدریج شروع شده و با گذشت زمان پیشرفت میکنند. این علائم به دو دسته اصلی حرکتی و غیرحرکتی تقسیم میشوند، که هر دو به یک اندازه بر کیفیت زندگی بیمار تأثیرگذارند.
| دستهبندی علائم | شرح و مثالها |
|---|---|
| علائم حرکتی (Motor Symptoms) | لرزش در حالت استراحت (Resting Tremor): لرزش ریتمیک (معمولاً ۴ تا ۶ بار در ثانیه) که اغلب از یک دست یا انگشتان شروع شده و زمانی که عضله در حالت استراحت است، رخ میدهد. این لرزش ممکن است شبیه به حرکت “چرخاندن قرص” بین انگشت شست و اشاره باشد و با حرکت هدفمند یا در خواب کاهش یابد. |
| کندی حرکات (Bradykinesia): دشواری در شروع حرکت و کاهش سرعت، دامنه و ریتم کلی فعالیتها. این علامت میتواند به صورت کاهش پلک زدن، “چهره بیحالت یا ماسکه” (Hypomimia)، کاهش چرخش بازوها هنگام راه رفتن و کوچک شدن دستخط (Micrographia) خود را نشان دهد. | |
| سفتی عضلات (Rigidity): انقباض و سفت شدن مداوم عضلات در دستها، پاها یا تنه که میتواند باعث درد، گرفتگی و محدودیت دامنه حرکتی شود. پزشک ممکن است هنگام حرکت دادن مفصل بیمار، یک مقاومت “چرخدندهای” (Cogwheel Rigidity) را احساس کند. | |
| مشکلات تعادل و وضعیت بدن (Postural Instability): این علامت معمولاً در مراحل بعدی بیماری ظاهر میشود و شامل خمیده شدن قامت (Camptocormia) و مشکل در حفظ تعادل است که خطر زمین خوردنهای مکرر را به شدت افزایش میدهد. | |
| علائم غیرحرکتی (Non-Motor Symptoms) | اختلالات خواب: بیخوابی، بیدار شدنهای مکرر، خوابآلودگی شدید در طول روز و اختلال رفتار در خواب REM (REM sleep behavior disorder) که فرد رویاهای خود را با حرکات فیزیکی خشن (فریاد زدن، لگد زدن) اجرا میکند و میتواند سالها قبل از علائم حرکتی بروز کند. |
| مشکلات روانی و خلقی: افسردگی بالینی، اضطراب فراگیر و بیتفاوتی (Apathy) یا از دست دادن انگیزه که بسیار شایع هستند و تأثیر عمیقی بر کیفیت زندگی بیمار و خانواده او دارند. | |
| مشکلات شناختی: اختلال در عملکردهای اجرایی مانند برنامهریزی، حل مسئله و تمرکز. در مراحل پیشرفتهتر، حدود ۳۰٪ بیماران ممکن است دچار زوال عقل (Dementia) شوند. | |
| مشکلات حسی و درد: از دست دادن یا کاهش قابل توجه حس بویایی (Anosmia) که یکی از اولین علائم بیماری است. درد مزمن، خستگی شدید و غیرقابل توضیح نیز بسیار شایع است. | |
| مشکلات سیستم عصبی خودکار: یبوست مزمن به دلیل کند شدن حرکات روده، افت فشار خون وضعیتی (Orthostatic Hypotension) که باعث سرگیجه شدید هنگام ایستادن میشود، مشکلات ادراری (تکرر یا فوریت ادرار) و اختلال در عملکرد جنسی. |
علل و عوامل خطر در بیماری پارکینسون
علت دقیق از بین رفتن سلولهای عصبی در پارکینسون هنوز به طور کامل شناخته نشده است، اما دانشمندان معتقدند که این بیماری نتیجه تعامل پیچیدهای بین استعداد ژنتیکی و محرکهای محیطی است.
- عوامل ژنتیکی: در حدود ۱۰ تا ۱۵ درصد از موارد، یک پیوند ژنتیکی قوی وجود دارد (پارکینسون خانوادگی). جهش در ژنهای خاصی مانند
SNCA،LRRK2(شایعترین)،PARK7،PINK1یاPRKNمیتواند خطر ابتلا را به میزان قابل توجهی افزایش دهد. برخی از این جهشها به صورت غالب (یک نسخه از ژن معیوب کافی است) و برخی به صورت مغلوب (دو نسخه از ژن معیوب لازم است) به ارث میرسند. با این حال، داشتن این جهشها لزوماً به معنای ابتلای قطعی به بیماری نیست و عوامل دیگری نیز باید نقش داشته باشند. - عوامل محیطی: قرار گرفتن در معرض برخی عوامل محیطی ممکن است خطر ابتلا را در افراد مستعد افزایش دهد. مطالعات اپیدمیولوژیک ارتباطاتی را بین بروز پارکینسون و تماس طولانیمدت با برخی سموم دفع آفات (مانند پاراکوات و روتنون)، علفکشها و فلزات سنگین نشان دادهاند. زندگی در مناطق روستایی و نوشیدن آب چاه نیز به عنوان عوامل خطر احتمالی مطرح شدهاند.
- سایر نظریهها: تحقیقات جدید بر روی سایر مکانیسمهای سلولی نیز متمرکز شدهاند. اختلال در عملکرد میتوکندریها (نیروگاههای سلول)، استرس اکسیداتیو (آسیب ناشی از رادیکالهای آزاد) و التهاب عصبی مزمن در مغز، همگی به عنوان فرآیندهایی شناخته میشوند که میتوانند به مرگ نورونهای دوپامینرژیک کمک کنند.
فرآیند تشخیص پارکینسون چگونه است؟

هیچ آزمایش خون یا تصویربرداری واحدی برای تشخیص قطعی پارکینسون وجود ندارد. تشخیص عمدتاً یک تشخیص بالینی است که توسط یک متخصص مغز و اعصاب باتجربه و بر اساس یک فرآیند دقیق انجام میشود.
- تاریخچه پزشکی و شرح حال: پزشک سؤالات دقیقی در مورد نوع علائم، زمان شروع آنها، سرعت پیشرفت و تأثیرشان بر زندگی روزمره میپرسد.
- معاینه عصبی: پزشک یک معاینه فیزیکی و عصبی کامل برای ارزیابی علائم اصلی پارکینسون انجام میدهد. از ابزارهایی مانند مقیاس رتبهبندی یکپارچه بیماری پارکینسون (UPDRS) برای ارزیابی شدت علائم حرکتی و غیرحرکتی به صورت کمی استفاده میشود.
- رد کردن سایر شرایط: بخشی از فرآیند تشخیص، رد کردن سایر بیماریهایی است که میتوانند علائمی شبیه به پارکینسون ایجاد کنند (پارکینسونیسم)، مانند عوارض جانبی برخی داروها، سکتههای مغزی کوچک متعدد، یا بیماریهای نادری مانند آتروفی چندسیستمی (MSA).
- پاسخ به دارو (آزمون لوودوپا): در برخی موارد، اگر تشخیص نامشخص باشد، پزشک ممکن است یک دوره آزمایشی داروی لوودوپا تجویز کند. بهبود قابل توجه علائم پس از مصرف این دارو، تشخیص پارکینسون را به شدت تأیید میکند.
- تصویربرداری تخصصی: یک نوع اسکن مغزی به نام DaTscan میتواند به تأیید تشخیص کمک کند. این اسکن از یک ماده رادیواکتیو برای اندازهگیری میزان ناقلهای فعال دوپامین (DAT) در مغز استفاده میکند. در بیماران پارکینسون، تراکم این ناقلها به طور مشخصی کاهش یافته است. این اسکن بیماری را تشخیص نمیدهد، اما میتواند آن را از شرایطی مانند لرزش اساسی که در آن سطح ناقل دوپامین طبیعی است، افتراق دهد.
آیا پارکینسون قابل درمان است؟ پاسخ قطعی
پاسخ کوتاه و صریح این است: خیر، در حال حاضر بیماری پارکینسون درمان قطعی و ریشهکنکننده ندارد. این یک بیماری مزمن و پیشرونده است، به این معنی که علائم آن با گذشت زمان بدتر میشود و نمیتوان روند اصلی بیماری (مرگ سلولهای عصبی) را به طور کامل متوقف یا معکوس کرد.
چرا پارکینسون در حال حاضر درمان قطعی ندارد؟
چالش اصلی در یافتن درمان قطعی، ماهیت پیچیده بیماری و موانع بیولوژیکی است. مغز انسان توسط سد خونی-مغزی (Blood-Brain Barrier) محافظت میشود که از ورود بسیاری از داروها و عوامل درمانی به مغز جلوگیری میکند. علاوه بر این، بازسازی یا جایگزینی سلولهای عصبی که از بین رفتهاند، یک چالش بزرگ علمی است. مهمتر از همه، تا زمانی که علائم حرکتی پارکینسون ظاهر شوند، بیمار پیش از این مقدار قابل توجهی (حدود ۶۰ تا ۸۰ درصد) از سلولهای تولیدکننده دوپامین خود را از دست داده است. این امر مداخله زودهنگام برای جلوگیری از آسیب را بسیار دشوار میسازد.
تمرکز درمانهای فعلی: کنترل علائم و بهبود کیفیت زندگی
اگرچه درمان قطعی وجود ندارد، اما این به معنای ناامیدی نیست. هدف اصلی تمام استراتژیهای درمانی موجود، مدیریت مؤثر علائم و حفظ بالاترین سطح کیفیت زندگی و استقلال عملکردی برای طولانیترین زمان ممکن است. درمانهای امروزی با جبران کمبود دوپامین، به مغز اجازه میدهند تا از منابع باقیمانده خود به طور مؤثرتری استفاده کند. این رویکرد میتواند به طور چشمگیری علائم حرکتی را کنترل کرده، به بیماران اجازه دهد تا سالها به فعالیتهای روزمره و حرفهای خود ادامه دهند.
روشهای درمانی و مدیریتی پارکینسون
مهم: انتخاب روش درمانی کاملاً به شرایط فردی بیمار، مرحله بیماری، شدت علائم و سبک زندگی او بستگی دارد. قبل از هرگونه اقدام درمانی، حتماً با پزشک متخصص مغز و اعصاب خود مشورت کنید.
درمانهای دارویی
داروها سنگ بنای درمان پارکینسون هستند و عمدتاً با هدف افزایش سطح دوپامین در مغز یا تقلید عملکرد آن کار میکنند.
| دسته دارویی | مکانیسم اثر | مثالها | نکات و عوارض جانبی شایع |
|---|---|---|---|
| لوودوپا (Levodopa) | مؤثرترین دارو؛ یک پیشساز دوپامین است که از سد خونی-مغزی عبور کرده و در مغز به دوپامین تبدیل میشود. معمولاً با کاربیدوپا ترکیب میشود تا از تجزیه آن در خارج از مغز جلوگیری کرده و عوارض جانبی را کاهش دهد. | Sinemet®, Madopar® | تهوع، سرگیجه، افت فشار خون. پس از مصرف طولانیمدت، ممکن است باعث نوسانات حرکتی (“on-off” fluctuations) و حرکات غیرارادی (دیسکینزی) شود. |
| آگونیستهای دوپامین | گیرندههای دوپامین را در مغز فعال کرده و عملکرد آن را تقلید میکنند. اغلب در بیماران جوانتر برای به تأخیر انداختن شروع لوودوپا استفاده میشوند. | پرامیپکسول، روپینیرول | خوابآلودگی ناگهانی، توهم، ورم پا، و ریسک رفتارهای تکانشی (مانند قماربازی، خرید افراطی یا پرخوری عصبی). |
| مهارکنندههای MAO-B | آنزیم مونوآمین اکسیداز B که دوپامین را در مغز تجزیه میکند، مهار میکنند و در نتیجه عمر دوپامین موجود را طولانیتر مینمایند. | سلژیلین، رازاگیلین | بیخوابی، سردرد، تهوع. میتوانند به تنهایی در مراحل اولیه یا همراه با لوودوپا استفاده شوند. |
| مهارکنندههای COMT | از تجزیه لوودوپا در بدن (قبل از رسیدن به مغز) توسط آنزیم COMT جلوگیری میکنند و در نتیجه اثربخشی هر دوز لوودوپا را افزایش میدهند. | انتاکاپون | اسهال، تغییر رنگ ادرار (قهوهای-نارنجی). همیشه همراه با لوودوپا مصرف میشوند. |
درمانهای جراحی
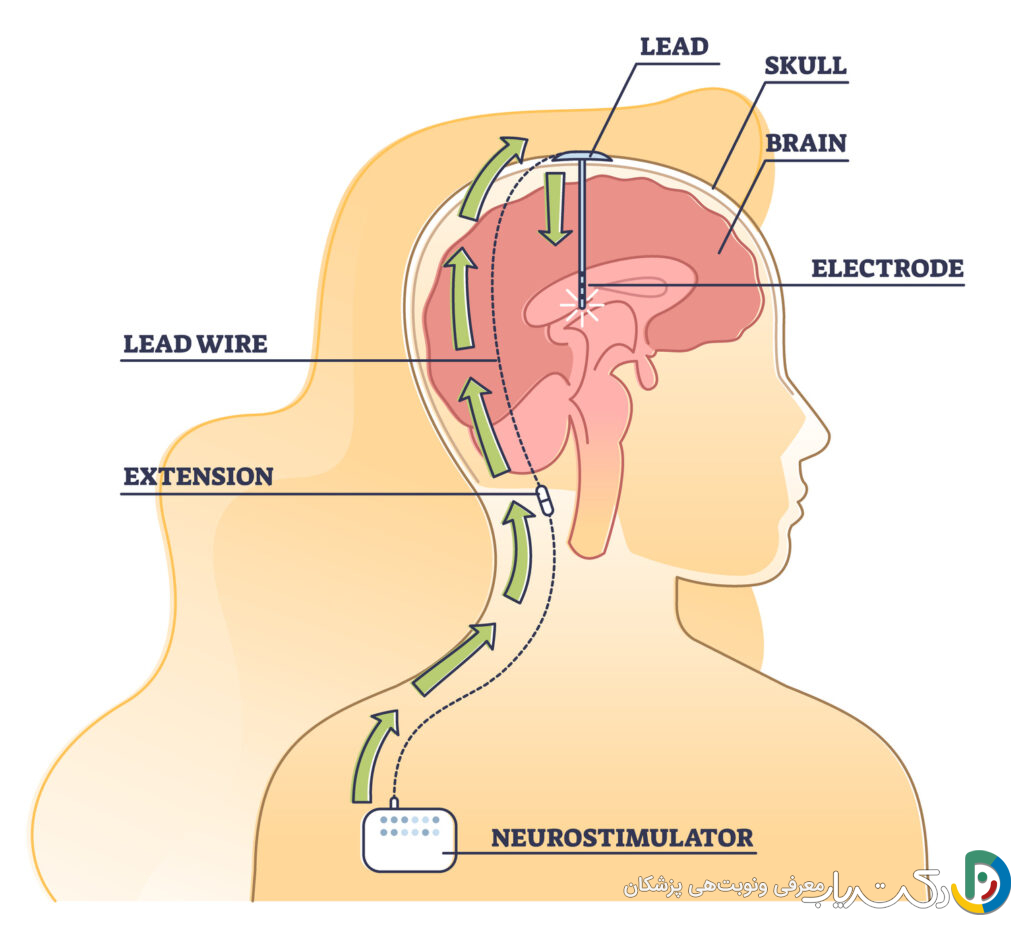
تحریک عمیق مغز (Deep Brain Stimulation – DBS): این روش که به “ضربانساز مغز” نیز معروف است، برای بیمارانی که دچار نوسانات حرکتی شدید یا دیسکینزی غیرقابل کنترل ناشی از داروها شدهاند، در نظر گرفته میشود. در این جراحی، الکترودهای بسیار نازکی در نواحی خاصی از مغز (مانند هسته سابتالامیک) کاشته میشود. این الکترودها به یک دستگاه ضربانساز که در زیر پوست قفسه سینه قرار میگیرد، متصل میشوند. این دستگاه پالسهای الکتریکی مداومی را برای تنظیم سیگنالهای غیرطبیعی مغز ارسال میکند و به این ترتیب به کنترل لرزش، سفتی و کندی حرکات کمک شایانی میکند، اما بر علائم غیرحرکتی تأثیر چندانی ندارد.
درمانهای توانبخشی
توانبخشی بخش جداییناپذیر و حیاتی مدیریت جامع پارکینسون است.
- فیزیوتراپی: تمرینات تخصصی مانند LSVT BIG به بهبود دامنه و اندازه حرکات کمک میکنند. تمرینات تعادلی، تمرینات راه رفتن و کشش برای مقابله با سفتی عضلات و کاهش خطر زمین خوردن ضروری هستند.
- کاردرمانی: به بیمار کمک میکند تا راهکارهایی برای انجام ایمن و آسان فعالیتهای روزمره پیدا کند. این شامل پیشنهاد وسایل کمکی، اصلاح محیط خانه و آموزش تکنیکهایی برای لباس پوشیدن یا غذا خوردن است.
- گفتاردرمانی: به رفع مشکلات بلع (Dysphagia) و بهبود قدرت و وضوح صدا که اغلب در بیماران پارکینسون ضعیف و تکصدا میشود، کمک میکند. برنامه درمانی LSVT LOUD یک استاندارد طلایی در این زمینه است.
سبک زندگی و درمانهای مکمل برای مدیریت پارکینسون
نقش تغذیه
یک رژیم غذایی سالم و متعادل میتواند به مدیریت علائم و بهبود سلامت عمومی کمک کند. رژیم غذایی مدیترانهای که سرشار از میوهها، سبزیجات، غلات کامل، ماهی و چربیهای سالم است، به دلیل خواص ضدالتهابی و آنتیاکسیدانیاش توصیه میشود. مصرف غذاهای غنی از فیبر و نوشیدن حداقل ۸ لیوان آب در روز برای مقابله با یبوست، که یک مشکل شایع در پارکینسون است، ضروری است. همچنین، برخی بیماران متوجه میشوند که مصرف وعدههای غذایی پرپروتئین میتواند در جذب داروی لوودوپا در روده اختلال ایجاد کند. به همین دلیل، توصیه میشود دارو حداقل ۳۰ دقیقه قبل یا یک ساعت بعد از وعده غذایی مصرف شود.
اهمیت ورزش
ورزش یکی از قدرتمندترین ابزارهای غیردارویی برای مدیریت پارکینسون است. تحقیقات نشان دادهاند که ورزش شدید و منظم نه تنها علائم را بهبود میبخشد، بلکه ممکن است اثرات محافظتکننده عصبی (Neuroprotective) داشته و روند پیشرفت بیماری را کندتر کند. یک برنامه ورزشی ایدهآل باید شامل چهار جزء باشد:
- تمرینات هوازی: (مانند پیادهروی سریع، دوچرخهسواری) برای سلامت قلب و عروق.
- تمرینات قدرتی: (مانند کار با وزنه) برای مقابله با ضعف عضلانی.
- تمرینات تعادلی: (مانند تای چی، یوگا) برای کاهش خطر زمین خوردن.
- تمرینات کششی و انعطافپذیری: برای کاهش سفتی عضلات.
آینده درمان پارکینسون: تحقیقات و امیدهای جدید
جامعه علمی به شدت در حال تحقیق برای یافتن درمانهای جدیدی است که بتوانند فراتر از مدیریت علائم عمل کرده و روند بیماری را اصلاح کنند.
- ژندرمانی: تلاش برای اصلاح یا جایگزینی ژنهای معیوب که باعث پارکینسون خانوادگی میشوند. چندین کارآزمایی بالینی در این زمینه در حال انجام است.
- درمان با سلولهای بنیادی: هدف این روش، جایگزینی نورونهای دوپامینرژیک از دست رفته با سلولهای جدید و سالمی است که از سلولهای بنیادی تمایز یافتهاند. این حوزه هنوز در مراحل اولیه تحقیق قرار دارد.
- ایمونوتراپی (Immunotherapy): توسعه واکسنها یا آنتیبادیهایی که سیستم ایمنی بدن را برای شناسایی و پاکسازی تودههای سمی پروتئین آلفا-سینوکلئین هدف قرار میده دهند تا از گسترش آنها در مغز جلوگیری کنند.
- پزشکی شخصیسازیشده: با درک بهتر زیرگروههای مختلف پارکینسون (بر اساس ژنتیک یا علائم)، درمانهای آینده احتمالاً به صورت شخصیسازیشده برای هر بیمار طراحی خواهند شد تا بیشترین اثربخشی را داشته باشند.
پرسشهای متداول (FAQ)
۱. میانگین سنی شروع بیماری پارکینسون چقدر است؟ معمولاً علائم پارکینسون پس از ۶۰ سالگی ظاهر میشوند. با این حال، حدود ۵ تا ۱۰ درصد از بیماران دچار “پارکینسون با شروع زودرس” (Young-Onset Parkinson’s Disease) میشوند که قبل از ۵۰ سالگی آغاز میگردد و اغلب پیشرفت کندتری دارد اما با دیسکینزی بیشتری همراه است.
۲. آیا استرس میتواند علائم پارکینسون را بدتر کند؟ بله، استرس روحی و جسمی میتواند به طور موقت و قابل توجهی علائم حرکتی، به ویژه لرزش را تشدید کند. هورمونهای استرس مانند کورتیزول میتوانند بر مدارهای حرکتی مغز تأثیر منفی بگذارند. به همین دلیل، تکنیکهای مدیریت استرس مانند مدیتیشن، یوگا و تنفس عمیق بخش مهمی از مدیریت بیماری هستند.
۳. آیا پارکینسون یک بیماری ارثی است؟ در اکثر موارد (حدود ۸۵-۹۰٪)، پارکینسون ارثی نیست و به صورت پراکنده (sporadic) رخ میدهد که نتیجه تعامل عوامل ژنتیکی و محیطی است. تنها در درصد کمی از بیماران، سابقه خانوادگی قوی و جهشهای ژنی مشخص به عنوان علت اصلی بیماری شناسایی میشوند.
۴. تفاوت بین لرزش پارکینسون و لرزش اساسی (Essential Tremor) چیست؟ افتراق این دو بسیار مهم است. لرزش پارکینسون معمولاً “لرزش در حالت استراحت” است که با حرکت هدفمند بهبود مییابد و اغلب با علائم دیگری مانند کندی حرکت و سفتی همراه است. در مقابل، لرزش اساسی یک “لرزش عملی یا وضعیتی” است که هنگام استفاده از دستها (مانند نوشتن یا نگه داشتن فنجان) بدتر میشود و معمولاً علائم دیگر پارکینسون را ندارد.
۵. امید به زندگی در بیماران پارکینسون چقدر است؟ با وجود درمانهای مؤثر امروزی، اکثر بیماران پارکینسون امید به زندگی طبیعی یا تقریباً طبیعی دارند. پارکینسون به خودی خود یک بیماری کشنده محسوب نمیشود. با این حال، در مراحل بسیار پیشرفته، عوارض ثانویه مانند ذاتالریه (به دلیل مشکلات بلع) یا آسیبهای ناشی از زمین خوردنهای شدید میتوانند تهدیدکننده زندگی باشند.
راهکارهای نهایی برای مدیریت پارکینسون
اگرچه پاسخ به سؤال “آیا پارکینسون قابل درمان است؟” در حال حاضر “خیر” است، اما این هرگز به معنای پایان راه نیست. چشمانداز مدیریت این بیماری در دهههای اخیر به کلی دگرگون شده است. امروزه، با یک برنامه درمانی جامع و شخصیسازیشده، افراد مبتلا به پارکینسون میتوانند زندگی طولانی، فعال و معناداری داشته باشند.
کلید موفقیت در مدیریت این بیماری، ایجاد یک تیم درمانی قوی و همکاری نزدیک بین بیمار، خانواده و متخصصانی چون متخصص مغز و اعصاب، فیزیوتراپیست، کاردرمانگر و گفتاردرمانگر است. مشارکت فعال بیمار در فرآیند درمان، پایبندی به داروها، انجام ورزش منظم و حفظ نگرش مثبت، همگی عواملی هستند که میتوانند به طور چشمگیری نتیجه درمان را بهبود بخشند. برای ارزیابی دقیق شرایط خود و تدوین بهترین برنامه مدیریتی، با پزشک متخصص مشورت کنید و به آیندهای روشنتر که با پیشرفتهای علمی رقم میخورد، امیدوار باشید.
منابع
NHS (UK). (2021). Parkinson’s disease. https://www.nhs.uk/conditions/parkinsons-disease/
Mayo Clinic. (2022). Parkinson’s disease. https://www.mayoclinic.org/
National Institute of Neurological Disorders and Stroke (NINDS). (2023). Parkinson’s Disease Information Page. https://www.ninds.nih.gov/
Parkinson’s Foundation. (n.d.). What Is Parkinson’s?. https://www.parkinson.org
The Michael J. Fox Foundation for Parkinson’s Research. (n.d.). Parkinson’s 101. https://www.michaeljfox.org/parkinsons-101
لیست پزشکان مرتبط:
- طیبه عباسیونمتخصص مغز و اعصاب (نورولوژی) | تهران
- مهدی سخابخشمتخصص مغز و اعصاب (نورولوژی) | تهران
- بابک زمانیمتخصص مغز و اعصاب (نورولوژی) | تهران
- رویا ابوالفضلیمتخصص مغز و اعصاب (نورولوژی) | تهران
- علیرضا رنجبر نائینیمتخصص مغز و اعصاب (نورولوژی) | تهران
- سید سهراب هاشمی فشارکیمتخصص مغز و اعصاب (نورولوژی) | تهران
- کلینیک مغز و اعصاب نورالیکلینیک مغز و اعصاب و نوروساینس | تهران
- ساناز معصومیمتخصص مغز و اعصاب (نورولوژی) | تهران
- مهران مهیارمتخصص مغز و اعصاب (نورولوژی) | تهران
- فاطمه شعبانیمتخصص مغز و اعصاب (نورولوژی) | تهران

